B7 同源物 4 蛋白(B7-H4)是 B7 家族中的一种跨膜糖蛋白,在正常健康组织中 B7-H4 处于相对低的表达水平,但在多种实体瘤中高表达。因此,B7-H4 也作为抗肿瘤治疗中具有潜力的靶点进行不断研发与探索。HS-20089 就是一种新型的以 B7-H4 为靶点的抗体药物复合物(ADC),在今年欧洲内科肿瘤学会(ESMO)大会上,复旦大学附属肿瘤医院张剑教授以优先口头报告的形式报告了该药物治疗实体瘤的初期数据(First-in-human/phase I trial of HS-20089, a B7-H4 ADC, in patients with advanced solid tumors,摘要号 381O)[1],丁香园肿瘤时间特邀张剑教授对该研究进行解读。
「 乘胜追击 」,剑指三阴性乳腺癌治疗新靶点
本次 ESMO 大会上公布了 HS-20089 首次人体试验的数据,Ⅰ 期试验阶段旨在评估 HS-20089 在晚期实体瘤中对于标准治疗无效的患者的耐受性、安全性、可耐受性、药代动力学和疗效,同时也评估剂量限制毒性(DLT)。合格的患者被纳入按剂量逐步递增队列(0.7 至 7.2 mg/kg)的 HS-20089 试验中,每 3 周静脉给药,并采用贝叶斯最优区间(BOIN)设计。
在本次报告上研究数据再次更新,截止到 2023 年 6 月 30 日,已有 52 名患有晚期实体瘤的患者接受了 HS-20089 治疗(其中 48 名乳腺癌患者,3 名卵巢癌患者和 1 名子宫内膜癌患者)。在其中的 2 名患者中观察到了 3 个 DLT(均出现在 7.2mg/kg 组)。最常见的治疗相关不良事件(≥20%)包括白细胞减少、中性粒细胞减少、恶心、贫血、血小板减少、呕吐、疲劳、丙氨酸氨基转移酶升高、食欲不振、天冬氨酸氨基转移酶升高和低钠血症,没有发现间质性肺病和输液反应。

图 1 安全性数据
在三阴性乳腺癌(TNBC)受试者中,潜在目标治疗剂量(4.8 和 5.8 mg/kg)下,TNBC 受试者 ORR 分别为 33.3% 和 27.3%,DCR 分别为 61.6% 和 81.8%。除此以外,既往接受过 PARP 抑制剂的 TNBC 患者 ORR 以及 DCR 分别为 75.0% 和 100%,既往接受过 PD-1/PD-L1 抑制剂治疗的 TNBC 患者 ORR 以及 DCR 分别为 42.9% 和 85.7%,提示 HS-20089 在 TNBC 后线治疗中的强大实力。
张剑教授谈道:「 在可评估疗效的 TNBC 患者中,总体有效率接近 30%,这一结果非常令人鼓舞。回顾 TNBC 的治疗格局,既 HER2、TROP2 之后,B7-H4 成为了全新具有治疗潜力的靶点。我们目前计划在剂量扩增队列中以进一步验证 HS-20089 在乳腺癌中的疗效,有望为乳腺癌患者提供更多治疗选择。」

图 2 TNBC 治疗数据
此外,HS-20089 在卵巢癌 (OC) 中显示出良好的抗肿瘤活性,在铂耐药 OC 中 ORR 为 66.7%,DCR 为 100%。
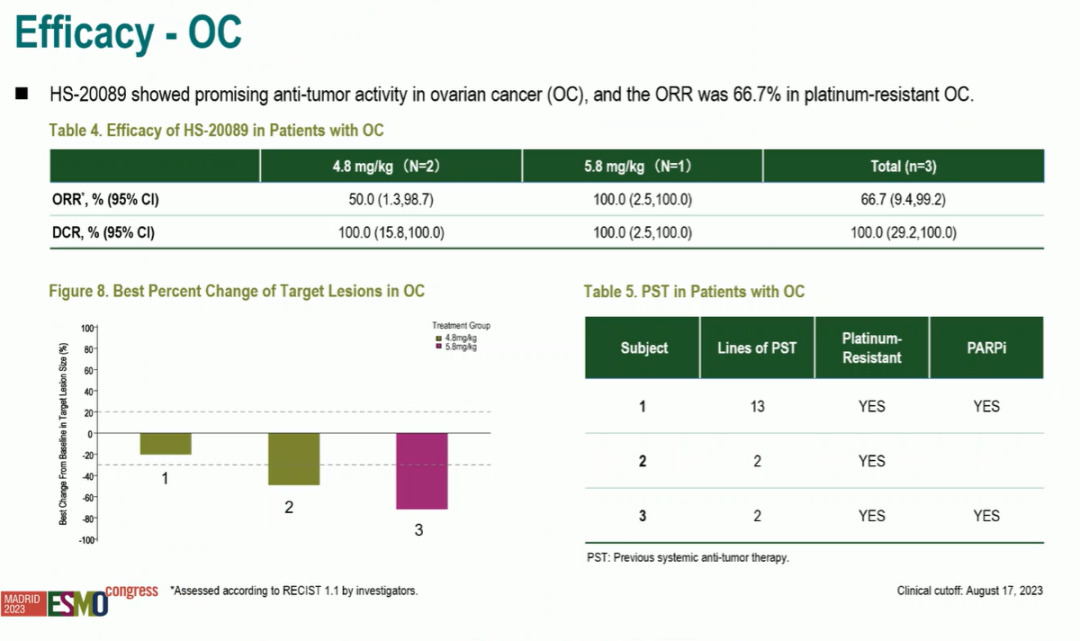
图 3 卵巢癌治疗数据
张剑教授谈道:「 从临床前研究到临床验证,目前披露的数据支持了 HS-20089 在实体瘤当中的继续探索。对于 HS-20089,未来的研究方向可能主要集中在乳腺癌,尤其针对 TNBC 的更大规模研究。如果数据可靠,未来也可能会向监管部门提交注册研究的申请。」
创新药物设计决定 HS-20089「 强劲 」 疗效
HS-20089 是一种新型的以 B7-H4 为靶点的抗体药物复合物(ADC),其结构包括一个人源化的抗 B7-H4 IgG1 单克隆抗体和一个小分子毒素拓扑异构酶 I 抑制剂,两者通过蛋白酶可切割的连接物相连,其载荷抗体比(DAR)为 6。DAR 决定了可以输送到肿瘤的 「 有效载荷 」,直接的影响了 ADC 的安全性和有效性。简单来说,ADC 的效果与 DAR 直接挂钩。DAR 可以理解为 ADC 这个魔法子弹所携带的载弹量,然而 DAR 的数值并不是越高越好。高 DAR 虽然拥有更大的载药量,但同时也更容易被人体的免疫系统锁定,从而被当成异物清除体外,减少 ADC 的有效性。而 HS-20089 让 DAR 数值保持在一个合适的点,兼具疗效的同时还保持有效性。
张剑教授谈道:「 该药物的创新性主要体现在两个方面。首先,它是第一个联合抗原的 ADC,这在目前的研究中还相对罕见。既往研究提示 B7-H4 调节 T 细胞的分化,抑制其分化为效应 T 细胞,介导肿瘤的免疫逃逸,因此 HS-20089 的治疗还有 『 一举两得 』 的优势。其次,除了乳腺癌,B7-H4 在多种肿瘤中表达较高,包括卵巢癌、子宫内膜癌等,因此 HS-20089 也有望成为泛癌种治疗策略之一。」
未来之路,ADC 仍是 「 一路繁花相送 」
在 TNBC 中已经涌现出多种 ADC,因此如何在这些选择中进行合适的选择、找到最佳的靶点以及开发伴随诊断工具都是重要的研究方向之一,这一发展为未来实现个体化治疗提供了更多机会。
张剑教授谈道:「ADC 的靶点已经非常多,除了 HER2、TROP2、B7-H4、B7-H3、EGFR 以及 Claudin18.2 等等,都在不同的肿瘤中显示出一定的相关性。在 ADC 的研发中,除了药物设计本身的重要性,临床前研究的探索对于选择合适的药物治疗也非常关键,同时选择合适的肿瘤类型也至关重要。我们期待未来在乳腺癌等实体瘤中有更多的药物支持相关治疗,最终希望患者能够从中受益。近年来,还有一些新型的 ADC 药物设计方式,比如双功能抗体等等。因此,未来可以看到 ADC 仍有良好的发展前景,我们所要做的就是耐心等待。」
总结而言,HS-20089 的研究为乳腺癌治疗领域带来了新的希望,也强调了在肿瘤治疗中继续寻找新的靶点和创新治疗方法的重要性。未来的研究将继续探索如何将这些新治疗方法整合到临床实践中,以实现更好的癌症治疗效果。
作者:uu;编辑:Huan
审核:张剑教授
题图:题库海洛plus
未经允许不得转载:CYQY-生活与科技 » 2023 ESMO | 张剑教授:新型 B7-H4 ADC 有望为多种难治瘤种提供新希望

 CYQY-生活与科技
CYQY-生活与科技