10 月 22 日,Thomas Powles 教授在欧洲肿瘤内科学会(ESMO)年会主席论坛报告 EV-302 研究结果并郑重宣布:「以前,我们从未在尿路上皮癌一线治疗中获得比化疗更好的生存结局,现在我们成功地实现了这一目标!」会场响起了如雷般的掌声,欢呼声不绝于耳。
EV-302 研究结果表明,相较于标准化疗,ADC+IO 方案可显著延长 OS(31.5 月 vs 16.1 月;HR 0.47)与 PFS(12.5 个月 vs 6.3 个月;HR 0.45)。该模式将成为新的晚期或转移性尿路上皮癌一线标准治疗。

Celebrate this milestone.
背景介绍
尿路上皮癌(UC)细胞高表达细胞粘附分子 Nectin-4 ,促进肿瘤细胞的生长。新型抗体-药物偶联物(ADC)Padcev(enfortumab vedotin,EV)由靶向 Nectin-4 的单克隆抗体与细胞毒制剂(单甲基奥瑞他汀 E,一种微管破坏剂)偶联而成,可特异性杀伤 UC 细胞。
此前,Padcev 在 EV-101(JCO,2020)、EV-201(Lancet Oncol,2021)、EV-301(NEJM,2021)研究中均验证了其作为二线治疗(先前接受过含铂化疗,或 PD-1/PD-L1 抑制剂治疗出现疾病进展)在局部进展或转移性 UC 患者中的疗效与安全性。基于此,伦敦玛丽女王大学巴茨癌症研究所 Thomas Powles 教授牵头开展了 EV-302/KEYNOTE-A39 研究,对比初治晚期或转移性尿路上皮癌接受 Padcev 联合帕博利珠单抗(EV+P)与标准治疗(化疗)的疗效与安全性,欲将 ADC 方案进一步推向晚期或转移性 UC 的一线治疗。
研究介绍
EV-302/KEYNOTE-A39 是一项开放标签、随机对照的 III 期研究,共纳入了 886 例既往未经治疗的晚期或转移性尿路上皮癌患者,中位随访时间达到 17.2 个月。在这项研究中,患者随机接受 ADC 联合 PD-1 抑制剂疗法或现有标准治疗(化疗)。本试验的双主要终点是根据盲态中心评审(BICR)依据 RECIST 1.1 标准确认的无进展生存期(PFS)和总生存期(OS)。
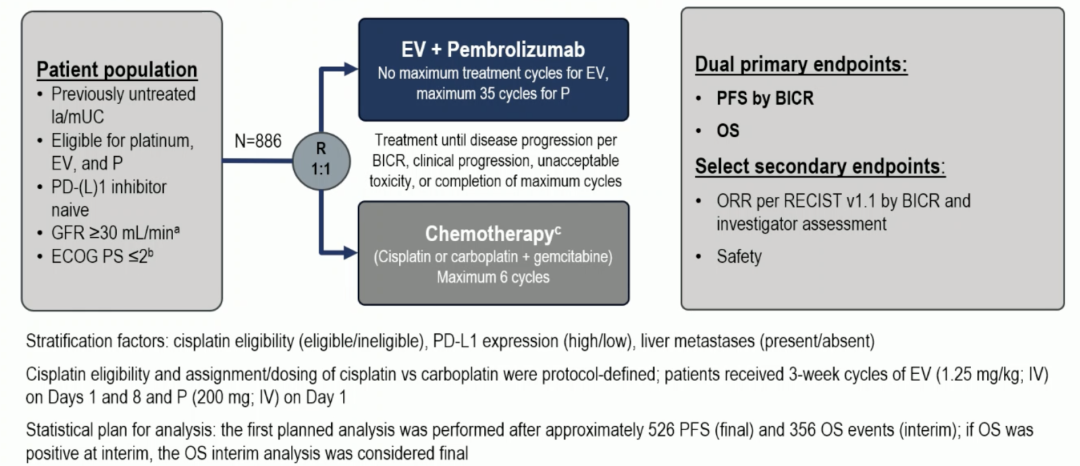
EV-302/KEYNOTE-A39 研究设计
研究结果
数据截止 2023 年 8 月 8 日,EV+P 方案相比一线标准化疗方案显著延长了晚期或转移性 UC 患者 mPFS,降低 55% 进展或死亡风险(mPFS:EV+P 12.5 个月 vs 化疗 6.3 个月;HR 0.45)。此外,ADC 联合免疫治疗的治疗模式在所有亚组分析中均优于标准化疗,无论 PD-L1 表达水平、原发灶部位、肝转移状态、ECOG 评分、是否可用顺铂等。
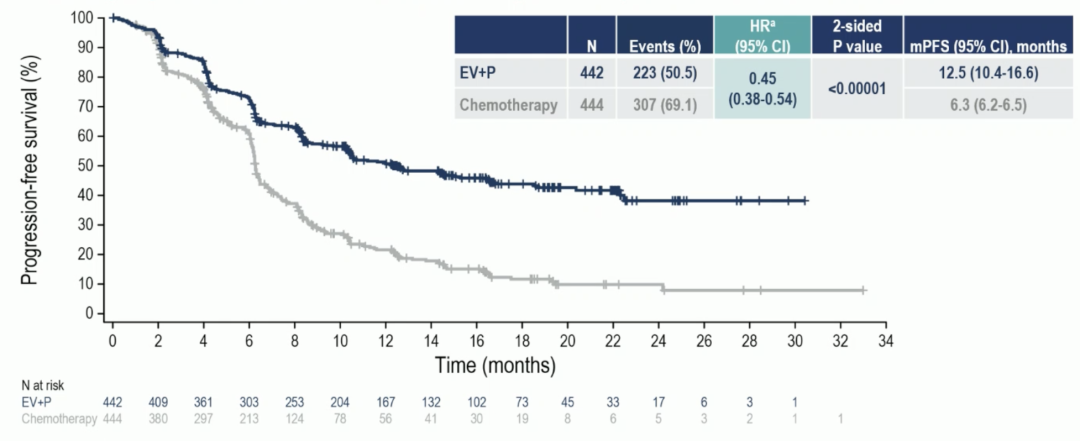
EV-302/KEYNOTE-A39 研究 PFS 结果
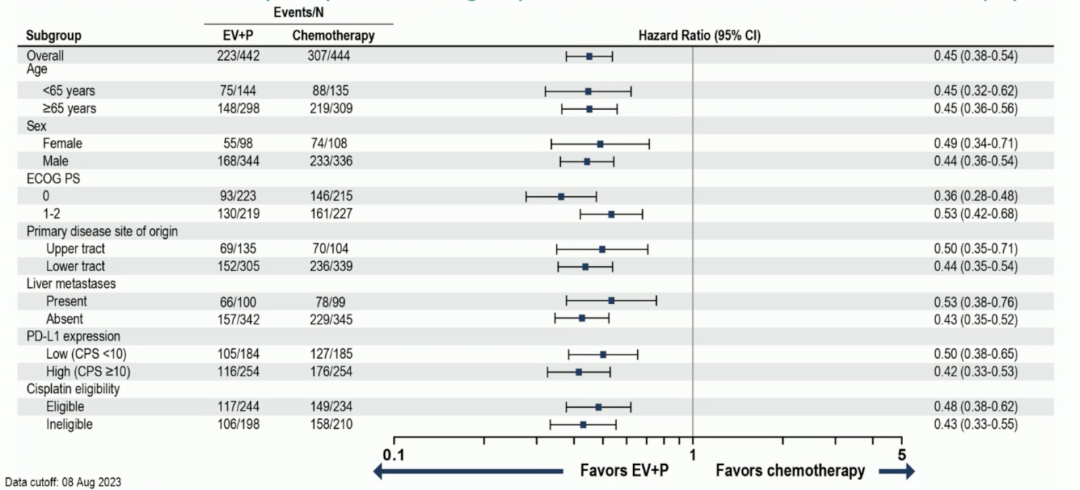
EV-302/KEYNOTE-A39 研究 PFS 亚组分析
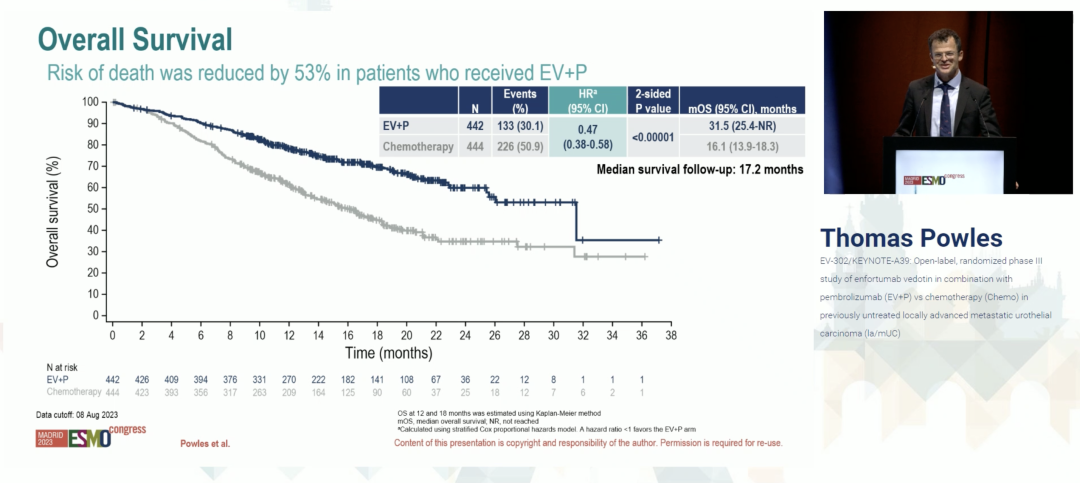
关于另一主要终点总生存期 OS,EV+P 组患者相较于接受标准化疗的患者显著延长了近一倍 OS,减少 53% 死亡风险(中位生存期 mOS:EV+P 31.5 个月 vs 化疗 16.1 个月;HR 0.47)。同样地,亚组分析结果显示,ADC 联合免疫的治疗模式相较于传统化疗的疗效总生存期优势不依赖于 ECOG 评分、原发灶部位、肝转移状态、PD-L1 表达、是否可用顺铂等。
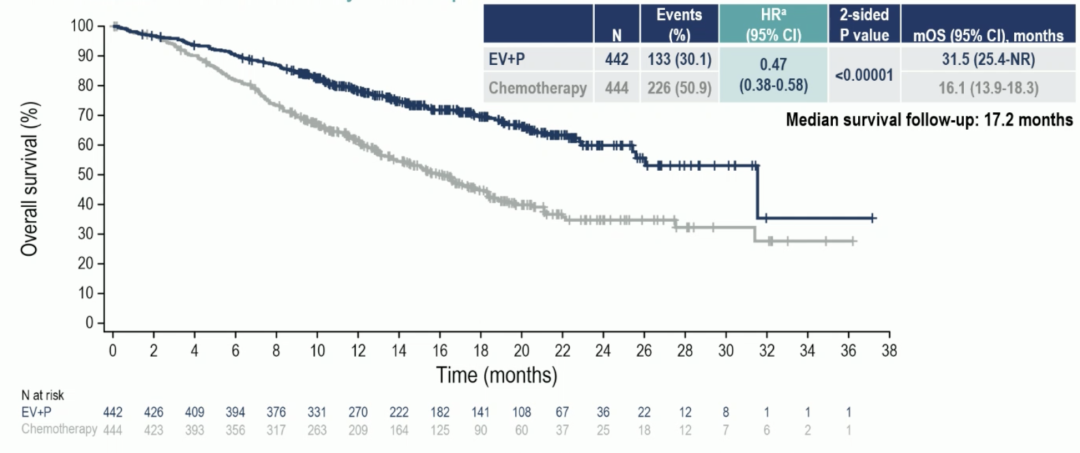
EV-302/KEYNOTE-A39 研究 OS 结果

EV302/KEYNOTE-A39研究OS亚组分析
EV+P 组客观缓解率(ORR)高达 67.7%,而传统化疗组的 ORR 为 44.4%。
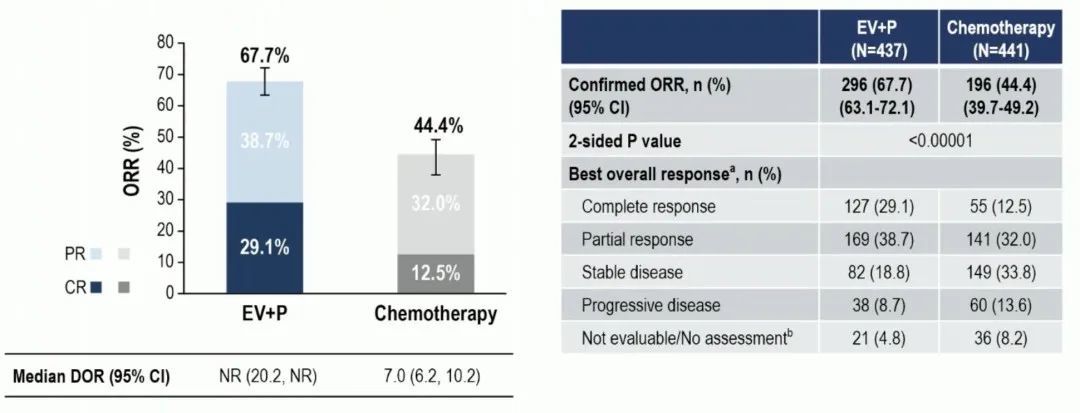
EV-302/KEYNOTE-A39 研究 ORR 结果
讨论
Andrea Apolo 教授在随后的讨论中指出,EV-302 研究的 ORR 为 67.7%,与此前在 EV-103 队列 A(ORR = 73.3%)和 EV-103 队列 K(ORR = 64.5%)中观察到的相似。EV+P 模式所达到的 mOS 、ORR 和 DoR 数据在所有的晚期或转移性尿路上皮癌的一线治疗临床研究达到最优,超越 CheckMate 901、IMvigor 130 以及 KEYNOTE 361 所代表的化免联合治疗模式,这意味着该模式将成为新的晚期或转移性尿路上皮癌的一线标准治疗!
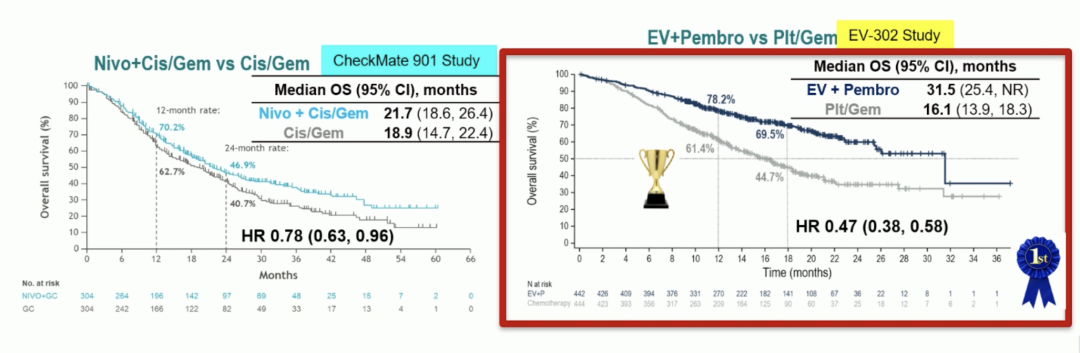
EV-302 与 CheckMate901 的 OS 对比

EV-302 与其他研究的 ORR 对比
安全性方面,ADC 联合免疫治疗模式的三级或以上不良反应总体发生率少于传统化疗组(EV+P 组和化疗组分别有 55.9% 和 69.5% 的患者发生 3 级或以上治疗相关不良反应)。其中,EV+P 组最常见的治疗相关不良反应为斑丘疹(7.7%)、高血糖(5.0%)和中性粒细胞减少症(4.8%);化疗组常见的治疗相关不良反应为贫血(31.4%)、中性粒细胞降低症(30.0%)和血小板减少症(19.4%)。整体而言,ADC 联合免疫治疗模式的安全性是可控的,且治疗期间未观测到新的不可预见的治疗相关不良反应。

EV-302 研究的安全性数据
该研究还分别探讨了 ADC 药物(EV)以及免疫治疗药物(P)所特别关注的治疗相关不良反应(TRAEs of special interest)。对于 EV 而言,特别关注的三级或以上治疗相关不良反应包括皮肤反应(15.5%)、周围神经病变(6.8%)和高血糖(6.1%)。对于 P 药而言,特别关注的三级或以上治疗相关突发不良反应为严重皮肤反应,其发生率在 11.8%。
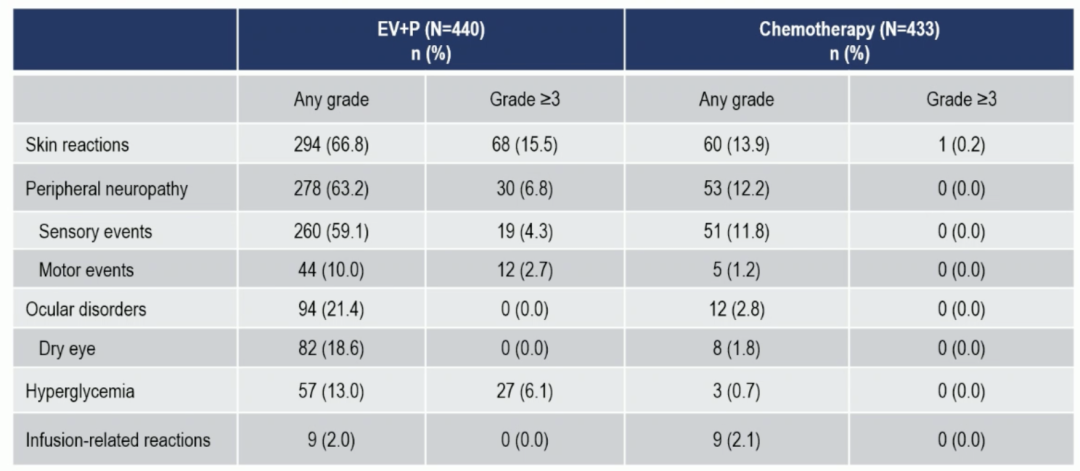
特别关注的 EV 治疗相关不良反应
结合疗效与安全性的结果可提示,基于 ADC 的联合治疗模式可能将为晚期或转移性尿路上皮癌患者带来「增效减毒」的临床获益。该研究具有划时代意义:EV+P 在一线未经治疗的晚期或转移性尿路上皮癌患者中击败标准化疗,延长了患者近一倍的生存期,同时兼具可控的安全性。晚期尿路上皮癌的一线治疗有望步入 ADC 联合免疫治疗的新时代!
本文首发于丁香园旗下专业平台:丁香园肿瘤时间
参考文献:
[1] Powles TB, et al. EV-302/KEYNOTE-A39: Open-label, randomized phase 3 study of enfortumab vedotin in combination with pembrolizumab (EV+P) vs chemotherapy (chemo) in previously untreated locally advanced metastatic urothelial carcinoma (la/mUC). ESMO Congress 2023, LBA6
[2] Rosenberg J, et al.. EV-101: A Phase I Study of Single-Agent Enfortumab Vedotin in Patients With Nectin-4-Positive Solid Tumors, Including Metastatic Urothelial Carcinoma. J Clin Oncol. 2020 Apr 1;38(10):1041-1049.
[3] Yu EY, et al. Enfortumab vedotin after PD-1 or PD-L1 inhibitors in cisplatin-ineligible patients with advanced urothelial carcinoma (EV‑201): a multicentre, single-arm, phase 2 trial. Lancet Oncol. 2021 Jun;22(6):872-882.
[4] Powles T, et al. Enfortumab Vedotin in Previously Treated Advanced Urothelial Carcinoma. N Engl J Med. 2021 Mar 25;384(12):1125-1135.
作者:Bryan;编辑:qxx
题图:站酷海洛 PLUS
未经允许不得转载:CYQY-生活与科技 » 首次击败化疗!31.5 vs 16.1 个月 OS,ADC+IO 实现 UC 生存翻倍

 CYQY-生活与科技
CYQY-生活与科技









