这款明星药,可能真的要被撤市了。
4 月 27 日,FDA 正式提议撤销安进 Tavneos® 的上市批准。
和此前 1 月的「请贵司自愿撤市」不同,本次 FDA 走的是行政撤市程序,最终能不能留在市场上,不再由安进说了算。
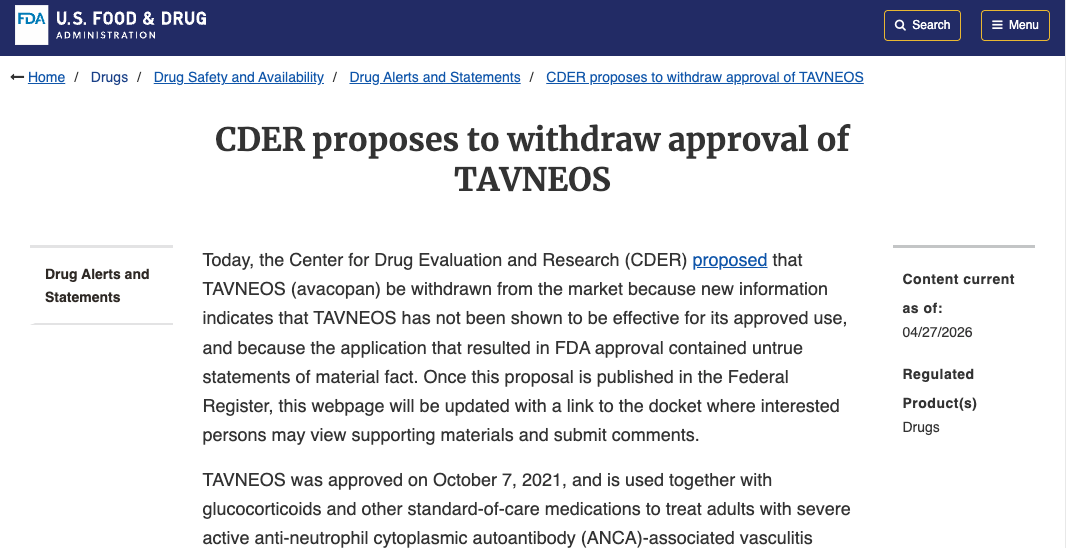
FDA 官网截图
自 2021 年获批上市以来,这款药陆续被报告与 76 例严重肝损伤存在因果关联,其中 54 人住院,8 人死亡。
这一次,FDA 动真格了。
8 死亡 54 住院,FDA 发函要求撤市
这次引发争议的药物,名称为 Tavneos®(avacopan),是安进旗下的一款口服补体 C5aR 抑制剂。
Tavneos® 主要用于治疗 ANCA 相关血管炎。这是一种因补体系统过度激活、最终导致广泛小血管破坏的罕见系统性自身免疫病。如果不及时治疗,往往危及生命。
在此之前,长期依赖激素+环磷酰胺/利妥昔单抗的经典方案。但长期大剂量使用糖皮质激素,副作用十分显著。
Tavneos® 作为目前唯一获批上市、针对严重活跃肉芽肿病伴多血管炎(GPA)和显微镜下多血管炎(MPA)的靶向口服治疗药物,它的核心卖点是「让患者少用激素」——这正切中了患者最迫切的临床痛点。
然而,Tavneos® 的争议,从获批起就从未停歇。
当年,FDA 批准 Tavneos® 上市,主要是基于其全球性关键 3 期 ADVOCATE 临床试验的数据。
根据伯明翰血管炎活动评分,该研究达到了第 26 周疾病缓解和第 52 周持续缓解的主要终点、糖皮质激素毒性显著降低、肾功能得到更大改善、与健康相关的生活质量指标也有较大改善。
虽然在疗效数据上基本过关,但 FDA 咨询委员会对该药的疗效数据投票结果却十分微妙——9:9,支持和反对打了个平手。
最终,公司于 7 月提交了该药市场推广申请的额外数据后,才得以通过 FDA 的快速通道上市。

公司公告
而众所周知,2021 年,正处于 FDA 快速审批程序最激进、最受争议的时间段内。名噪一时的阿尔茨海默病药物 Aduhelm,在咨询委员会以 10:0 投票反对批准的情况下,仍然通过加速审批通道获批,三名委员会成员随后愤而辞职。
Tavneos® 的上市,也正是在同一时期。
到了今年年初,Tavneos® 的问题迎来集中暴发。
1 月,FDA 发函对 Tavneos® 提出 2 点问题:
问题一:数据完整性
3 期临床 ADVOCATE 试验中,对 331 名受试者里 9 名患者的主要终点结果进行了重新裁定,FDA 对这一操作过程存疑。
所谓「重新裁定」,指的是在试验结束、数据揭盲之后,对其中 9 名患者的终点结果又重新评估了一遍,改变了原来的判定结论,有可能会影响整体疗效数据结果。
问题二:肝毒性
该药的肝损伤问题是已知风险,但 FDA 认为在重新审视整体获益-风险时,这一风险权重需要重新考量。
根据 FDA 4 月公布数据,已在全球范围内确认了 76 例与 Tavneos® 使用有合理因果关系的药物性肝损伤(DILI)病例,包括住院(n=54)和死亡(n=8)。

FDA 公告
据此,FDA 要求药企「自愿将 Tavneos® 撤出美国市场」,但安进公司在 12 天后便回应暂不打算撤市,表示:
「目前未发现临床试验的基础患者数据存在问题,且在审查相关临床数据及多年真实世界证据后,有信心证明 Tavneos® 具有疗效和良好的获益-风险比。」
最新文件披露,申报材料「关键事实造假」
4 月 27 日,FDA 把这场撤市对峙正式升级为行政撤市程序。在这次的撤市提案里,FDA 详细复盘了 ADVOCATE 试验当年到底发生了什么。
ADVOCATE 试验的关键终点是「第 52 周持续缓解率」,要求药物组优于对照组、且差异具有统计学显著性。这其中,患者是否缓解,由独立的裁定委员会来判断。
2019 年 11 月 5 日,ADVOCATE 试验数据库第一次锁定并揭盲。分析结果显示原始 p 值=0.1025,没达到统计学显著,按这个结果药批不下来。
公司先把数据重新核查了一遍,但数据没错,分析也没错,就是 p 值不显著。其间,公司首席医学官给生物统计学总监发了一封邮件,明确写道:「我们不能错过这里的优效性结果。」
于是公司换了个思路,既然数据没法挑,那就挑患者。
生物统计学总监在已揭盲的数据库里挑出 9 名处在「判定边界」上的患者,他们的病情看起来压住了(伯明翰血管炎活动评分为 0),但因为最近用过激素,按规则被判为未缓解。
内部测算显示,如果这 9 个人里有 5 个被改判成缓解、对照组不变,统计学显著就能达成。随后,这 9 个人的病例资料被再次送到裁定委员会主席手里,重新裁定。
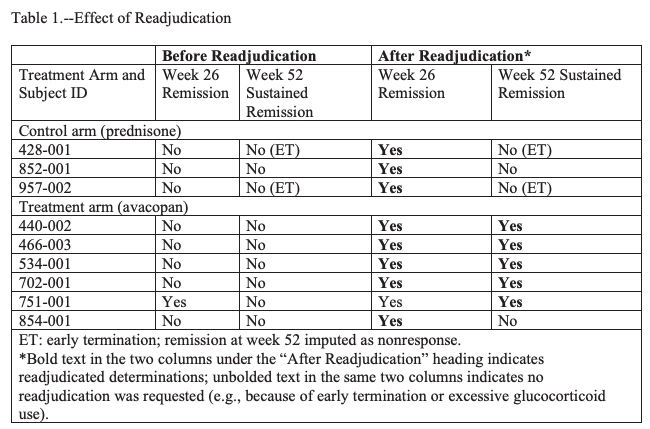
9 名患者重新裁定前后的缓解状态对比,粗体为改判后的结论。(图源:FDA 文件截图)
结果跟公司预算的一模一样,有 5 名患者被改判成缓解,这个结果让数据实现了翻盘——p=0.0132。
而在最终提交给 FDA 的申请文件里,只报告了 0.0132 这个数字,完全没提此前失败的 0.1025。
对此,FDA 措辞极为严厉:「申请材料含重大事实不实陈述」。
不仅如此,FDA 还在提案里披露,当年主审团队并不建议批准 Tavneos®,是部门主任顶住主审意见、依据「持续缓解的统计学优效结果」才批的。
「如果部门主任知道这些事实,他不会建议批准。」FDA 这样写道。
此外,Tavneos® 的安全性问题也再次引发关注。
在最新提案中,FDA 再次强调,目前已确认了 7 例胆管消失综合征(VBDS),其中 3 例死亡,但 VBDS 在 Tavneos® 上市前未被识别,原始标签中亦无相应警示。
37 亿美元,真的要打水漂了吗?
Tavneos® 并非安进自研。2022 年,安进以每股 52 美元、总计 37 亿美元收购了药企 ChemoCentryx,同时将 Tavneos® 收入囊中。希望「能够通过 Tavneos® 在炎症和肾脏病学领域积累数十年领导地位,变革 ANCA 相关血管炎治疗方案」。
此后,安进拿下了该药在亚洲及拉丁美洲(含中国内地)的商业化权益。前后投入可谓不低。
但上市 5 年来,Tavneos® 的销售数据其实算不上好。
2025 全年,Tavneos® 卖出约 4.6 亿美元,而安进总收入达到了 351 亿,Tavneos® 占比仅 1.3%,算不上是主要产品。
尽管如此,安进 CEO 在 2024 年致股东信中依然将其描述为「正在成为 ANCA 血管炎重要治疗选择」的药物。
如果在此时主动撤市,不仅意味着承认并购失败,37 亿美元打了水漂,还要面对被追责和诉讼的连锁风险。
安进在官网更新事件进展
对于 FDA 的撤市提案,安进反应非常迅速。仅两天后的 4 月 29 日,安进向 FDA 提交了 Tavneos® 标签更新申请,主动加入 VBDS 警告。
有评论认为,安进此举旨在主动承认安全信号,以削弱 FDA 「安全性失控」的指控。
按程序,接下来安进可以申请听证会为自己辩护,申请截止日期为 2026 年 6 月 1 日。
但需要明确的是,按照现在的流程,如果 FDA 认为安进提交的材料不足以构成「真实且实质性的重大事实争议」,甚至可以直接撤市,连听证会都不用开。

策划:z_popeye|监制:islay
特别声明:以上文章内容仅代表作者观点,不代表本站观点或立场。如有关于作品内容、版权或其它问题请于作品发表后与我们联系。

 CYQY-生活与科技
CYQY-生活与科技