全球最高级别的肿瘤学领域会议第 60 届美国临床肿瘤学会(ASCO)年会已于美国东部时间(GMT-5)2024 年 5 月 31 日~6 月 4 日在美国芝加哥举行。会上,北京大学肿瘤医院齐长松教授口头汇报了两项 CAR-T 细胞疗法(以下简称「CAR-T」)治疗胃肠道肿瘤研究数据(摘要号:2501 和 2518),在国际舞台唱响中国之声。
「丁香园肿瘤时间」特邀齐长松教授针对这两项研究结果接受专访,探讨 CAR-T 治疗胃肠道肿瘤的进展。
重点提炼
①Abstract 2501:Claudin 18.2 CAR-T 细胞治疗用于胃肠道肿瘤患者:CT041-CG4006 I 期临床试验最终结果。
②Abstract 2508:GUCY2C CAR-T 细胞治疗 IM96 用于转移性结直肠癌患者的 I 期研究。
晚期胃肠道肿瘤治疗选择有限,亟待探索新型免疫治疗策略
晚期胃癌(GC)和转移性胰腺癌预后差,治疗选择有限,CLDN18.2 是 CLDN18 紧密连接蛋白的胃特异性亚型,在消化系统肿瘤中高度表达,是抗肿瘤治疗的潜在靶点[1]。CT041是一种靶向 Claudin 18.2 自体 CAR-T 细胞,临床试验(NCT03159819)表明 CT041 具有良好的耐受性,可能成为胃癌和胰腺癌患者的新的治疗选择[1]。
转移性结直肠癌(mCRC)治疗预后欠佳,尤其是肝转移患者,鸟苷酸环化酶 2C(GUCY2C)在不同阶段结直肠癌中异常表达,并且局限于肠道[2]。IM96 是靶向GUCY2C 靶点的自体 CAR-T 细胞产品,研究(NCT05287165)显示 IM96 具有良好的耐受性并显示出令人鼓舞的疗效,但疗效与肿瘤的 GUCY2C 表达水平、输注剂量和 CAR-T 扩增水平相关,还需进一步探索[2]。
CAR-T 细胞疗法的靶向抗原选取要点
齐长松教授强调,「对于 CAR-T 来讲,往往是将肿瘤表面的膜蛋白作为靶向抗原。首先,我们要求所选抗原在肿瘤细胞中有比较高的表达,其次这个靶点要在正常组织是有限的表达,从而利用表达的差别能够识别肿瘤细胞,同时不攻击正常的细胞。Claudin 18.2、GUCY2C 就符合上述特征,可作为 CAR-T 细胞疗法的靶向抗原。」
CT041-CG4006 I 期临床试验最终结果:样本量提升,队列得以扩展
ORR 和DCR 分别达 38.8%和 91.8%,安全性可控
2022 年 5 月 9 日,齐长松教授团队在国际权威学术期刊 Nature Medicine 在线发表了论文「Claudin18.2-specific CAR T cells in gastrointestinal cancers: phase 1 trial interim results」,研究中期分析报告了 CT041 在 37 例 CLDN18.2 阳性的晚期胃肠道(GI)肿瘤患者中展现出良好的安全性和颇具前景的有效性,特别是在胃癌(GC)患者中[1]。
2024 年 6 月 3 日,齐长松教授团队的论文「Claudin18.2-specific CAR T cells in gastrointestinal cancers: phase 1 trial final results」再次见刊国际权威学术期刊Nature Medicine[3],与此同时,齐教授在本次 ASCO 年会上报告了这项试验的最终结果[4]。
这项单臂、开放标签、I 期试验评估了 CT041 在 CLDN18.2 阳性晚期 GI 肿瘤患者中的安全性和有效性。齐长松教授表示,首先相较于之前公布的中期分析,研究的样本量有明显的提升,从之前的 37 例患者到现在的 98 例患者。在更大的人群里看到了 CT041 作为新兴治疗方法的安全性及有效性。
其次,研究探索了更多的队列,试验采用「3 + 3」设计进行剂量递增(250 × 106、375 × 106、500 × 106 或 1000 × 106 个细胞),CT041 在 4 个队列中进行扩展(队列 1:CT041 用于接受过治疗的晚期 GI 肿瘤患者,队列 2:CT041 + PD-1 单抗治疗用于接受过治疗的晚期 GI 肿瘤患者,队列 3:胃癌一线治疗后序贯 CT041,队列 4:CT041 用于既往抗 CLDN18.2 抗体治疗失败的患者)。研究的主要终点为安全性,次要终点为根据 RECIST v1.1 标准评估的有效性、药代动力学和免疫原性。
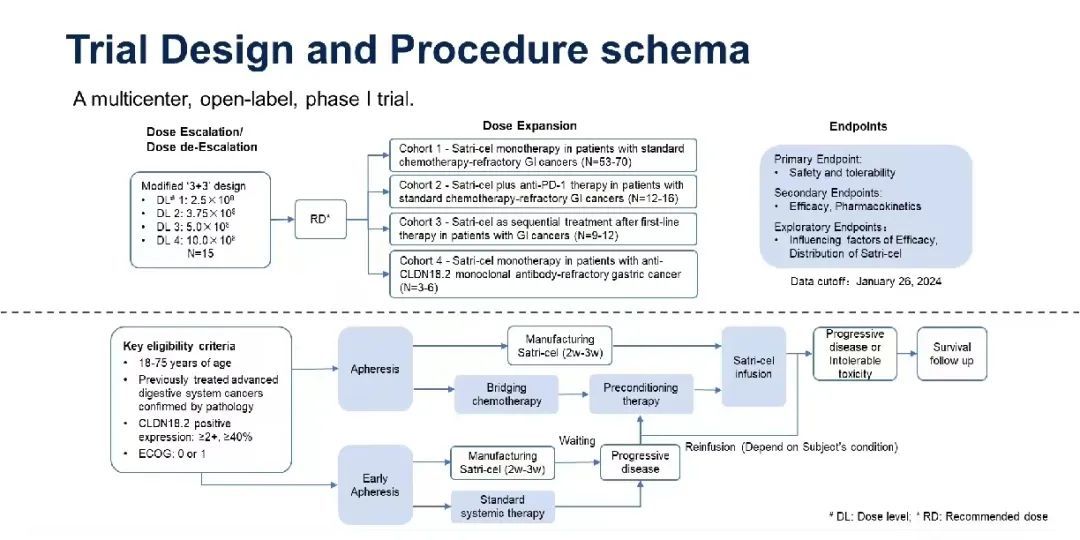
图 1.试验设计(来自讲者幻灯)
从 2019 年 3 月 26 日至 2024 年 1 月 26 日,共有 98 例患者接受了 CT041 输注,包括胃癌(n = 73 例)、胰腺癌(n = 10 例)、胆道癌(n = 4 例)、肠癌(n = 8 例)和其他肿瘤(n = 3 例)。共有 89 例患者接受了 250 × 106 个细胞的剂量,6 例患者接受了 375 × 106 个细胞,3 例患者接受了 500 × 106 个细胞,中位随访时间为 29.7 个月(1.2~35.5 个月)。
齐长松教授表示 CT041 的安全性是非常可控的,没有非常严重的不良反应。最常见 ≥ 3 级治疗相关不良事件是与淋巴细胞耗竭相关的血液学毒性,未报告剂量限制性毒性、治疗相关死亡或免疫效应细胞相关神经毒性综合征。细胞因子释放综合征发生在 96.9% 的患者中,全部为 1~2 级。8 例(8.2%)患者中发现胃黏膜损伤,包括 7 例 1~2 级和 1 例 3 级糜烂性胃炎,患者该症状已恢复。
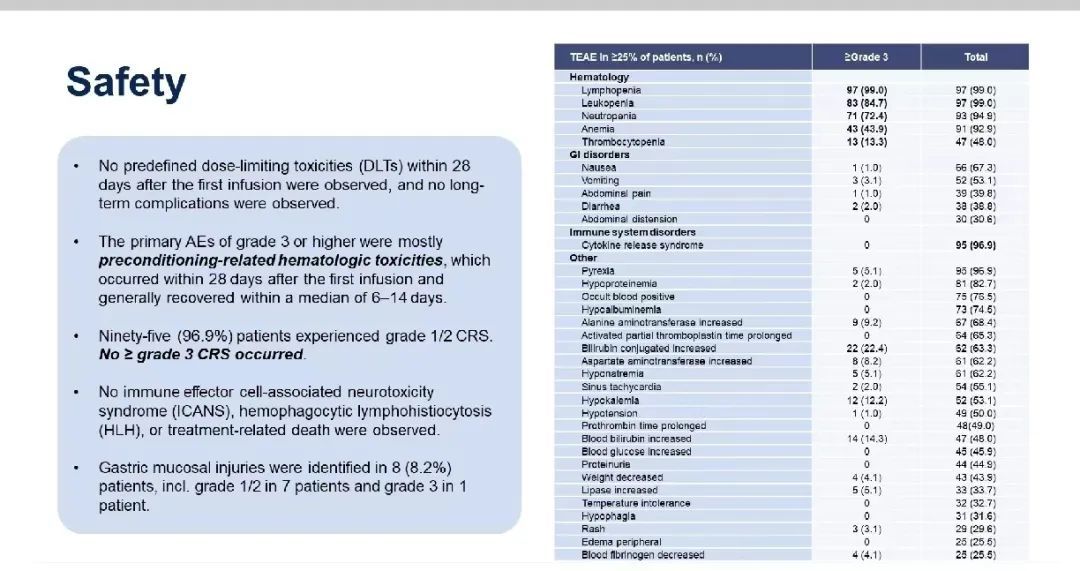
图 2.CT041 的安全性(来自讲者幻灯)
齐长松教授表示,研究显示,在不同的队列、不同的瘤种中,CT041 的有效性都是非常确切的。所有患者(n = 98)的客观缓解率(ORR)和疾病控制率(DCR)分别达到 38.8% 和 91.8%。所有患者的中位无进展生存期(PFS)和中位总生存期(OS)分别为 4.4 个月(3.7~6.6 个月)和 8.8 个月(7.1~10.2 个月)。
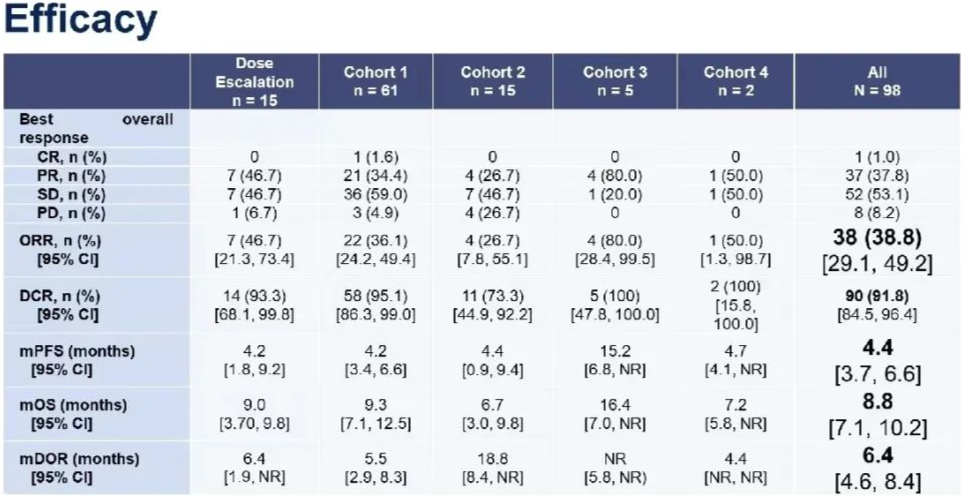
图 3.CT041 的疗效(来自讲者幻灯)
在接受 CT041 单药治疗的疗效可评估的胃癌患者中,有可测量病灶患者(n = 47例)的 ORR 和 DCR 分别达 57.4% 和 83.0%,所有疗效可评估的胃癌患者(n = 55)的中位 PFS 和中位 OS 分别为 5.8 个月(4.2~8.4 个月)和 9.7 个月(7.1~14.4 个月)。
IM96 治疗 mCRC 患者的I期研究结果更新:DL3 中 ORR 达 40%
疗效持久,安全性可控
2023 年欧洲肿瘤学会(ESMO)大会上,齐长松教授团队公布了 IM96 剂量爬坡阶段的数据,当时只入组了 9 例患者。本次 ASCO 年会,齐长松教授团队更新了研究的数据[5]。齐长松教授表示,「首先,研究有样本量的扩大,截止到目前,已入组 20 例患者,我们在更大的人群当中评估了 IM96 的安全性和有效性。其次,根据在前期已经结束的剂量爬坡阶段数据,选择剂量梯度 3 作为扩展剂量,在扩展队列已入组了 8 例的 mCRC 患者」。这项开放标签、3 + 3 设计、剂量递增研究纳入了至少接受过 ≥ 3 线治疗的 GUCY2C 阳性 mCRC 患者。患者预先接受氟达拉滨(Fludarabine)和环磷酰胺治疗,然后接受一次 IM96 输注,剂量为 3 × 108(DL1)、6 × 108(DL2)、12×108(DL3)或 20 × 108(DL4)CAR-T 细胞。研究者在 DL3 进行了剂量扩展研究。研究的主要终点为安全性和毒性,次要终点为疗效和药代动力学特征。
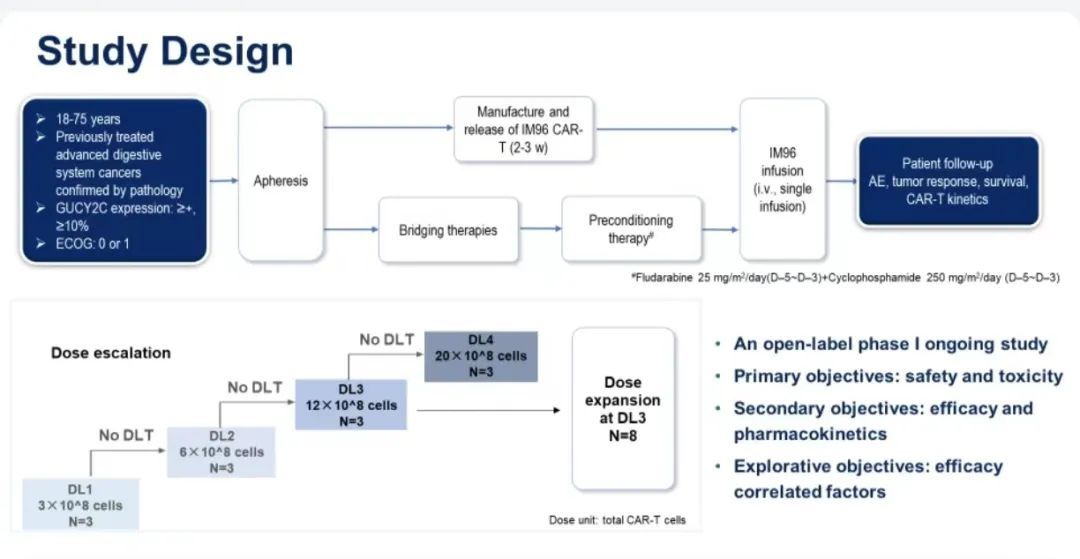
图 4.研究设计(来自讲者幻灯)
所有患者的随访时间为 7~19 个月,患者中位年龄为 52.5 岁,11/20 例患者(55%)为男性,11/20 例患者(55%)存在肝转移,20/20 例患者(100%)错配修复功能完整(pMMR),12/20 例患者(60.0%)KRAS 突变,1/20 例患者(5.0%)NRAS 突变,3/20 例患者(15.0%)BRAF 突变,19 例患者接受了桥接治疗。
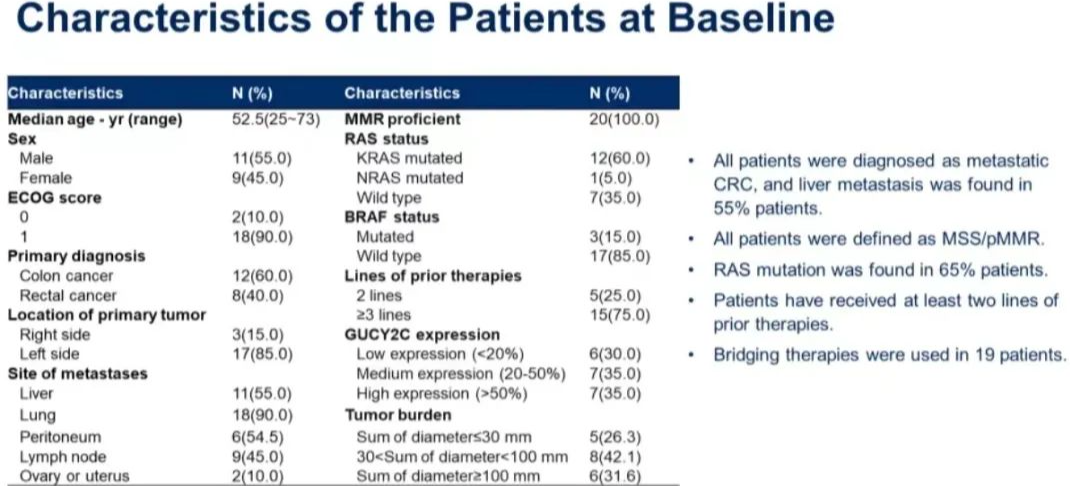
图 5.患者的基线特征(来自讲者幻灯)
仅 1/20 例患者(5.0%)出现神经毒性和 ≥ 3 级细胞因子释放综合征(CRS)。16/20 例患者(80.0%)出现 1~2 级 CRS,白细胞介素-6 显著增加。14/20 例患者(70.0%)观察到 1~3 级皮疹。11/20 例患者(55.0%)出现 3 级腹泻,7/20 例患者(35.0%)仅在 DL2、DL3 和 DL4 组中出现 1~3 级口腔黏膜炎,未出现剂量限制毒性和最大耐受剂量。
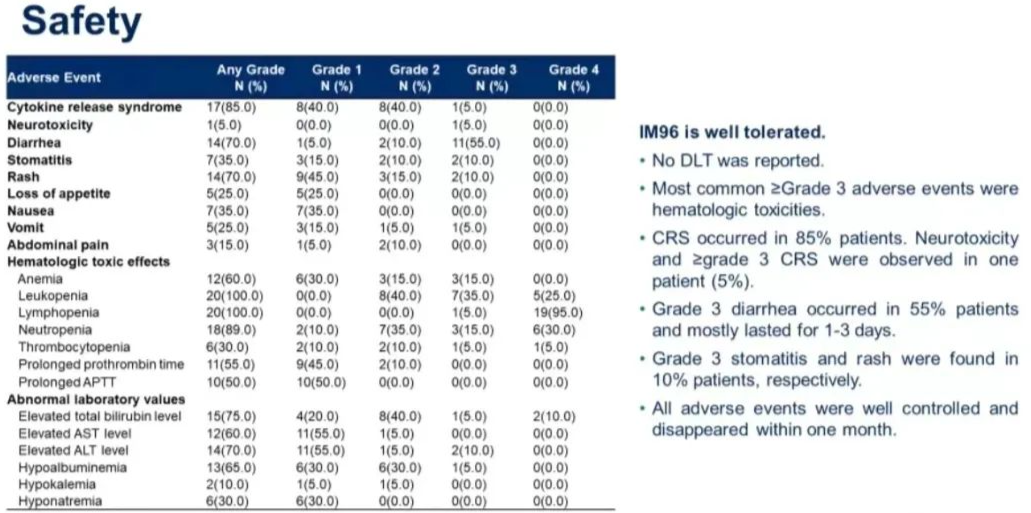
图 6.IM96 的安全性(来自讲者幻灯)
在 19 例可评估疗效的患者中,DCR 为 73.7%,ORR 为 26.3%。齐长松教授表示,在 DL3 组中,无论是否发生肝转移,患者的 ORR 为 40.0%,较去年公布的 ORR(仅 11%左右)有明显提升。DL3 组的中位 PFS 为 7 个月,中位缓解持续时间(DoR)为 10 个月。在 6 个月内没有缓解的患者出现疾病进展。所有患者的肿瘤缓解与癌胚抗原(CEA)水平显著降低相关。
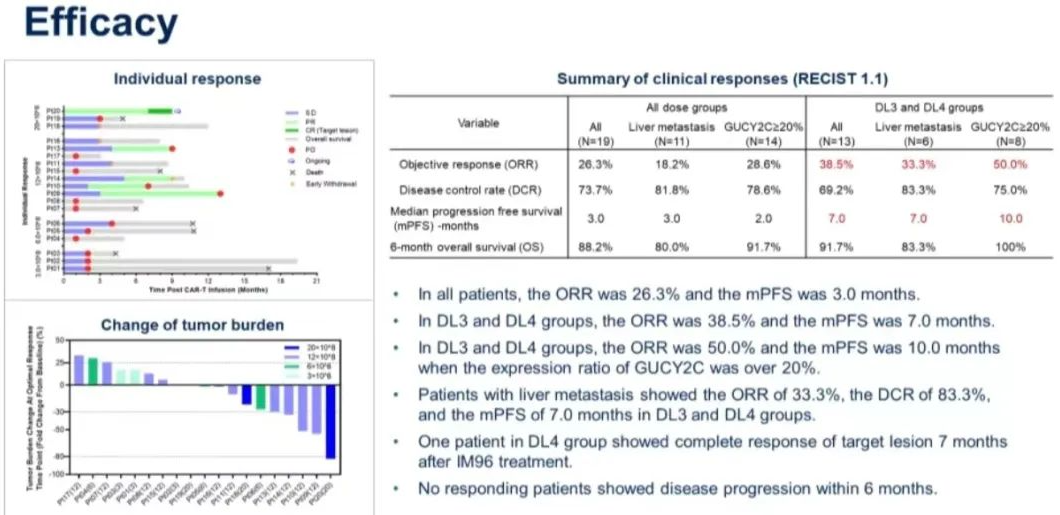
图 7.IM96 的有效性(来自讲者幻灯)
胃肠道肿瘤 CAR-T 治疗,前景广阔,未来可期
齐长松教授
提到,「近年来,具备特定靶点的 CAR-T 治疗在晚期胃肠道肿瘤治疗中迎来了突破。主要表现在两个方面,一方面是既往 CAR-T 治疗在实体瘤中的探索非常少,我们对不良反应的管控缺乏经验,怕出现严重的不良反应。近年来,随着大量 CAR-T 临床试验开展,我们对于不良反应的管控积累了经验,有规范的处理流程,可快速地在很大的人群中去探索 CAR-T 治疗。另一方面 CAR-T 作为一种新兴的疗法,国内的不同公司或医院层面的投入越来越多,目前开发细胞治疗的企业在国内像雨后春笋一般成长,并且关注的靶点也是多种多样的,在实体瘤的临床试验的开展非常多,因此开创了一个实体瘤细胞治疗的快速发展时期。上述两个研究均显示 CAR-T 治疗在胃肠道肿瘤领域展现出巨大的潜力,未来可期」。
总结与展望
CT041 在 CLDN18.2 阳性晚期 GI 肿瘤患者中 ORR 和 DCR 分别达38.8% 和 91.8%,显示出有前景的疗效和可控的安全性,期待在不同的队列进一步扩大样本量,以指导今后 CT041 治疗的策略及临床试验的设计;对 CT041 输注后T细胞亚群的动态监测、CT041 对患者生活质量的影响有待于进一步研究。IM96 在 DL3 pMMR mCRC 患者队列中的 ORR 为 40%,具有持久的疗效和可接受的安全性,特别是在肝转移患者中显示出高度的抗肿瘤潜力。IM96 疗效相关因素的转化研究有限,期待进一步研究,提高疗效,实现精准治疗。
采访嘉宾

齐长松 教授
北京肿瘤医院一期临床病区 副主任医师 医学博士
主要从事实体瘤细胞免疫治疗、消化系统肿瘤的规范化诊疗和个体化治疗
中国临床肿瘤学会(CSCO)胃肠间质瘤专委会委员、秘书
中国临床肿瘤学会(CSCO)青年专家委员会委员
北京癌症防治学会胃癌防治专委会秘书长
中国老年医学学会肿瘤学分会委员
中国医促会胃肠外科学分会委员
《肿瘤综合治疗电子杂志》编委
《Health Care Science》青年编委
审校:齐长松教授
整理:暖暖;编辑:Bree
题图:图虫创意
未经允许不得转载:CYQY-生活与科技 » 齐长松教授:两项 CAR-T 治疗胃肠道肿瘤前景广阔|ASCO 2024 中国之声

 CYQY-生活与科技
CYQY-生活与科技









