循环肿瘤 DNA (ctDNA) 在早期膀胱癌领域是一种潜在的生物标志物,但在晚期尿路上皮癌(UC)中应用较少[1]。Ⅲ 期临床试验 KEYNOTE-361(NCT02853305)旨在探索帕博利珠单抗联合化疗 vs. 帕博利珠单抗单药 vs. 单纯化疗(chemo)治疗晚期 UC 患者的疗效及安全性。2021 年,KEYNOTE-361 的最终数据在 Lancet Oncology 公布,显示在晚期 UC 患者的一线含铂化疗中添加帕博利珠单抗并未改善疗效[2]。近些年来,针对 KEYNOTE-361 的探索性分析不断开展。
在今年的美国临床肿瘤学会(ASCO)年会上,来自英国巴兹癌症研究所的
Prof.Thomas Powles
公布了帕博利珠单抗单药组和单纯化疗组的临床结局以及基于治疗前和治疗期间的 ctDNA 检测数据进行的回顾性分析结果
[1]
。「丁香园肿瘤时间」特邀
Prof.Thomas Powles
基于此次研究数据接受专访,探讨 ctDNA 在晚期 UC 诊疗领域的应用价值。
KEYNOTE-361 研究:阴性结果带来积极思考
KEYNOTE-361 研究共纳入 1010 例未经治疗的晚期 UC 患者,这些患者按照 1:1:1 的比例随机分配至帕博利珠单抗单药组(302 例)、帕博利珠单抗 + 化疗组(349 例)、单纯化疗组(342 例)。
在采访中,谈及研究结果,
Prof.Thomas Powles
表示,KEYNOTE-361 这项临床试验的结果是阴性的,即没有达到预先设定的主要终点
[3]
。尽管如此,从免疫治疗的疗效角度来看,无论是联合治疗还是免疫单药治疗,都显示出一定的抗肿瘤活性。大约有 20% 的患者在接受免疫治疗后出现了持久的缓解,但目前还无法确定哪些患者会从中受益。总体来说,这项试验虽然没有达到预设终点,但为特定UC人群提供了免疫治疗、免疫联合化疗疗效的潜在支持性证据。同时,将本试验结果与其他试验相比较可能有助于进一步理解上述治疗方法的潜在价值和局限性。
大浪淘沙留是金,再启 ctDNA 探索性分析
在 2024 ASCO 年会的这项新公布的论文中,帕博利珠单抗单药组和单纯化疗组的部分患者被纳入 ctDNA 探索性队列分析,这些患者将在基线或治疗第 1 周期(C1,治疗前)和治疗第 2 周期(C2,治疗期间)分别接受 ctDNA 检测。ctDNA 探索性队列分析的主要终点为自基线起或治疗期间 ctDNA 水平的变化(定义为 maxVAF)是否与最佳总缓解(BOR)、无进展生存期(PFS)、总生存期(OS)等临床结局相关,次要终点为在调整组织肿瘤突变负荷(tTMB)、程序性死亡蛋白-配体 1(PD-L1)等多个变量后,基线至 C2 的 maxVAF 变化是否与临床结局相关
[1]
。
最终,共有 263 例患者被纳入 ctDNA 探索性队列分析,单纯化疗队列 131 例,帕博利珠单抗单药队列 132 例。
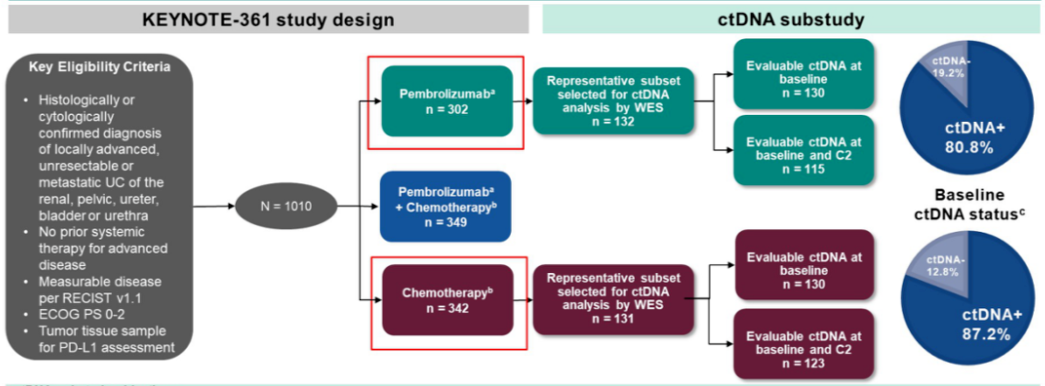
图 1.KEYNOTE-361 研究设计(来自讲者幻灯)
结果显示,两个队列的临床特征和基线 ctDNA 水平相似,大多数患者基线 ctDNA 为阳性表达。
基线 ctDNA 水平与临床结局的相关性
在帕博利珠单抗队列中,C1 时 ctDNA 水平(maxVAF)较低与更好的 ORR、PFS 和 OS 相关(P < 0.01),并且在调整 TMB 和 PD-L1 后仍保持相关性;但这一相关性在化疗队列中未达到显著性(P > 0.05)。这表明,基线 ctDNA 水平与帕博利珠单抗治疗的临床结局相关,但与化疗的临床结局无关。
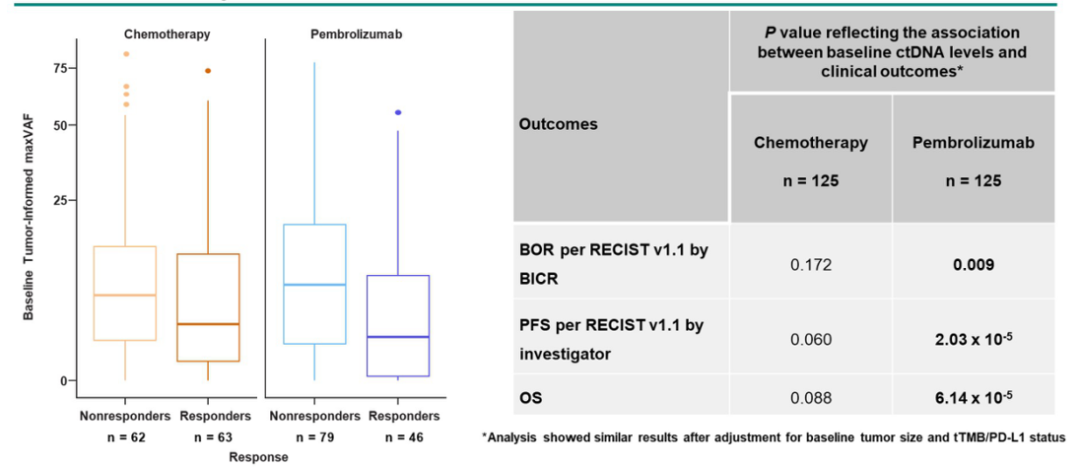
图 2.不同治疗下基线 ctDNA 水平与临床结局的相关性(显著性预设为 α = 0.05;来自讲者幻灯)
不同治疗队列之间的 C1 至 C2 的 ctDNA 水平变化
与帕博利珠单抗队列相比,化疗队列 C1 至 C2 的 ctDNA 水平降低幅度更大;使用分子反应(MR)评分也观察到了类似的结果。由此可见,化疗导致的 ctDNA 水平自基线到 C2 的下降幅度(包括 ctDNA 清除率)大于帕博利珠单抗治疗导致的 ctDNA 水平下降幅度。
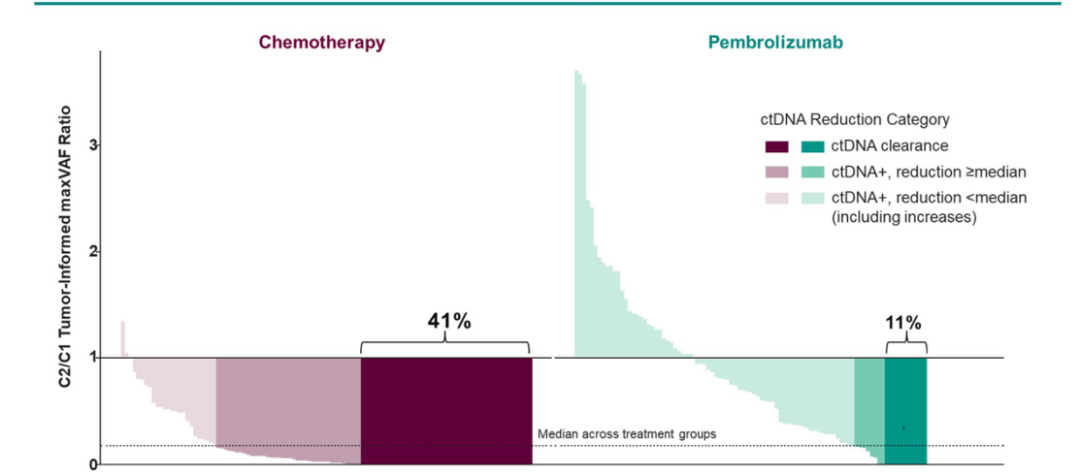
图 3.C1 至 C2(C2/C1)的 ctDNA 改变及清除率(来自作者幻灯)
C1 至 C2 的 ctDNA 水平变化与临床结局的相关性
化疗队列的 ctDNA 水平降低与 ORR、PFS(P < 0.001)和 OS(P < 0.01)改善显著相关;MR 评分与 ORR 和 PFS 显著相关(P < 0.01)。在帕博利珠单抗队列中,这一相关性更强(P < 0.001),并且在调整 TMB 和 PD-L1 后仍保持相关性。
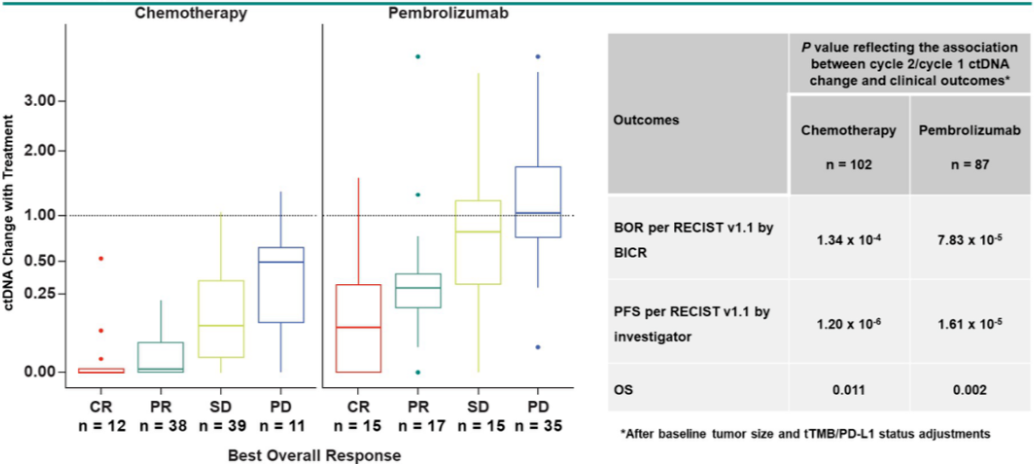
图 4.不同治疗下 C2/C1 ctDNA 改变和清除率与临床结局之间的相关性(显著性预设为α = 0.05;来自讲者幻灯)
帕博利珠单抗治疗导致的 ctDNA 变化与长期结局相关性更高,并且在高 tTMB 和 PD-L1 水平高表达人群中,短期 ctDNA 水平下降并不能作为临床结局的独立性临床替代终点。
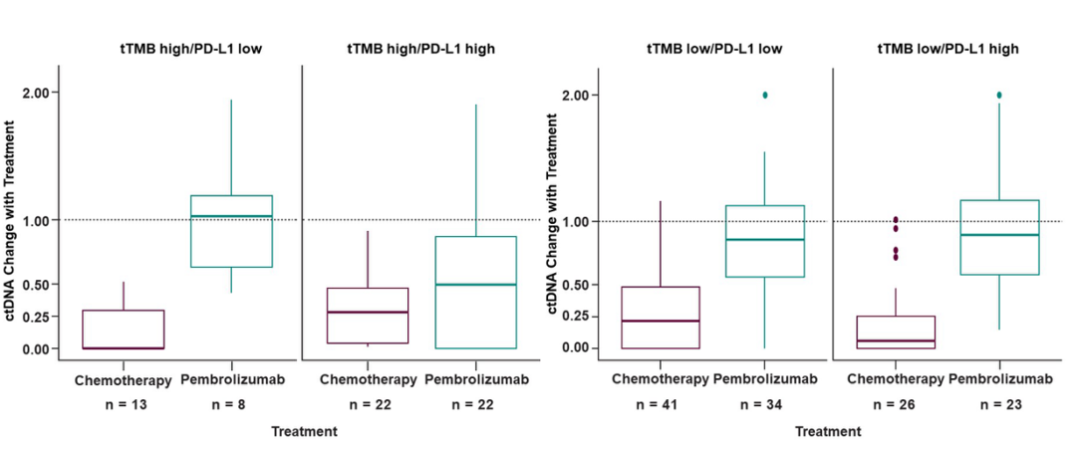
图 5.不同 tTMB、PD-L1 水平、治疗下的 ctDNA 变化与临床结局的相关性(来自作者幻灯)
与化疗队列中 ctDNA 水平下降幅度较大的患者相比,帕博利珠单抗队列中 ctDNA 水平下降幅度较大的患者 OS 数据更有利。
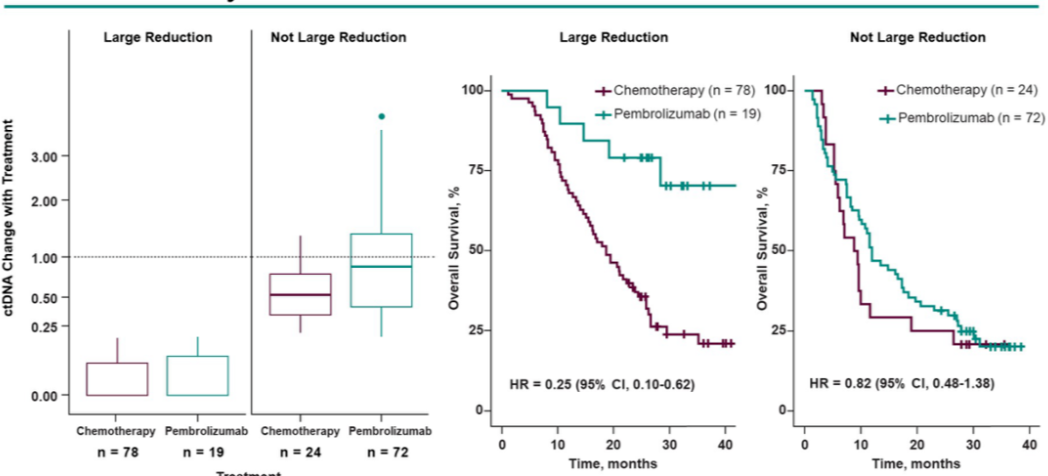
图 6.不同治疗下 ctDNA 下降幅度与 OS 的相关性(来自作者幻灯)
研究者认为,本次分析结果证实,ctDNA 动力学可以受到治疗机制的影响,这一结论将有助于未来在联合治疗策略的深入探索。
ctDNA 可作为预测晚期 UC 患者预后的生物标志物
谈及本次分析的最新结果,Prof.Thomas Powles 提到,「我们发现,ctDNA 水平自 C1 至 C2 的变化与患者的临床结局相关。ctDNA 水平的变化可以作为治疗反应的早期预测指标,并且可以帮助医疗团队制定更有效的治疗策略。尽管 ctDNA 似乎在这个研究背景下并没有带来实践性的改变,但是它提供了重要信息:大部分患者 ctDNA 检测都是阳性的。ctDNA 的基线水平与帕博利珠单抗治疗后的疗效相关,ctDNA 基线水平较低者预后更佳。这表明基线 ctDNA 水平可作为一个用于分层的生物标志物,对于化疗和帕博利珠单抗治疗的疗效都有影响,尤其是在较低水平时。
因此,我们认为,ctDNA 水平可作为晚期 UC 患者的预后生物标志物,因为在不同ctDNA 水平的人群之间比较时,ctDNA 水平较低的患者总体上预后较差」。
生物标志物探索困难诸多,详尽规划、规避局限性
在谈及本次探索性分析的困难与挑战时,Prof.Thomas Powles 表示,「在尿路上皮癌生物标志物探索过程中,我们面临的第一大挑战是需要制定一个明确的研究计划。因为在该试验中,我们将进行成百上千次的分析,以期能最终发现一些具有临床意义的结果。因此,我们预先需有一个非常详尽和全面的分析计划。此外,病人数量及失访也是需要考虑的限制性因素。最后,ctDNA 检测方法有很多种,本研究中仅使用了 Guardant 方法,还有其他方法可以使用。
同时,我们关注到,在探索过程中随着时间的推移,ctDNA 水平不断变化,我们需要纳入更多时间窗下的患者肿瘤或组织标本。我认为,在针对的 UC 的其他疗法中,ctDNA 水平的变化及其相关价值也值得期待」。
采访嘉宾

Thomas Powles 教授
英国伦敦大学巴兹癌症中心
伦敦大学泌尿科癌症教授
巴兹癌症中心主任
Annals of Oncology 主编
欧洲内科肿瘤学会(ESMO)理事会成员
ESMO 非泌尿生殖道前列腺癌指南(2020-2023 版)主编
欧洲泌尿外科协会(EAU)肾癌指南主编
曾任ESMO、ESMO IO、ESMO Asia 和 EMUC 教育和科学指导委员会主席
荣获 2018 年 ASCO GU 的膀胱癌年度奖项
整理:张帆;编辑:Bree
未经允许不得转载:CYQY-生活与科技 » ctDNA 能预测晚期尿路上皮癌预后!英国学者 Thomas Powles ASCO 现场专访

 CYQY-生活与科技
CYQY-生活与科技









